Nouveau traitement pour l'arthrose du genou
La prise en charge de l'arthrose du genou entre dans une phase de transformation sans précédent. Alors que les traitements conventionnels -- anti-inflammatoires, infiltrations de corticoïdes, viscosup...
La prise en charge de l'arthrose du genou entre dans une phase de transformation sans précédent. Alors que les traitements conventionnels -- anti-inflammatoires, infiltrations de corticoïdes, viscosupplémentation -- se limitent à soulager temporairement la douleur sans modifier l'évolution de la maladie, une nouvelle génération de thérapies vise désormais à réparer le cartilage, moduler l'inflammation articulaire et, dans certains cas, régénérer les tissus détruits. Plasma riche en plaquettes, cellules souches mésenchymateuses, biothérapies anti-cytokines, thérapie génique, implants de cartilage cultivé en laboratoire, prothèses imprimées en 3D : le paysage thérapeutique de la gonarthrose se transforme en profondeur. Certains de ces nouveaux traitements pour l'arthrose du genou sont déjà accessibles en pratique clinique, tandis que d'autres progressent rapidement dans les essais cliniques de phase II et III. Cet article fait le point sur chacune de ces approches, leur niveau de preuve, leur disponibilité et ce que les patients peuvent en attendre concrètement.
Le PRP (plasma riche en plaquettes) : un nouveau traitement pour l'arthrose du genou déjà accessible
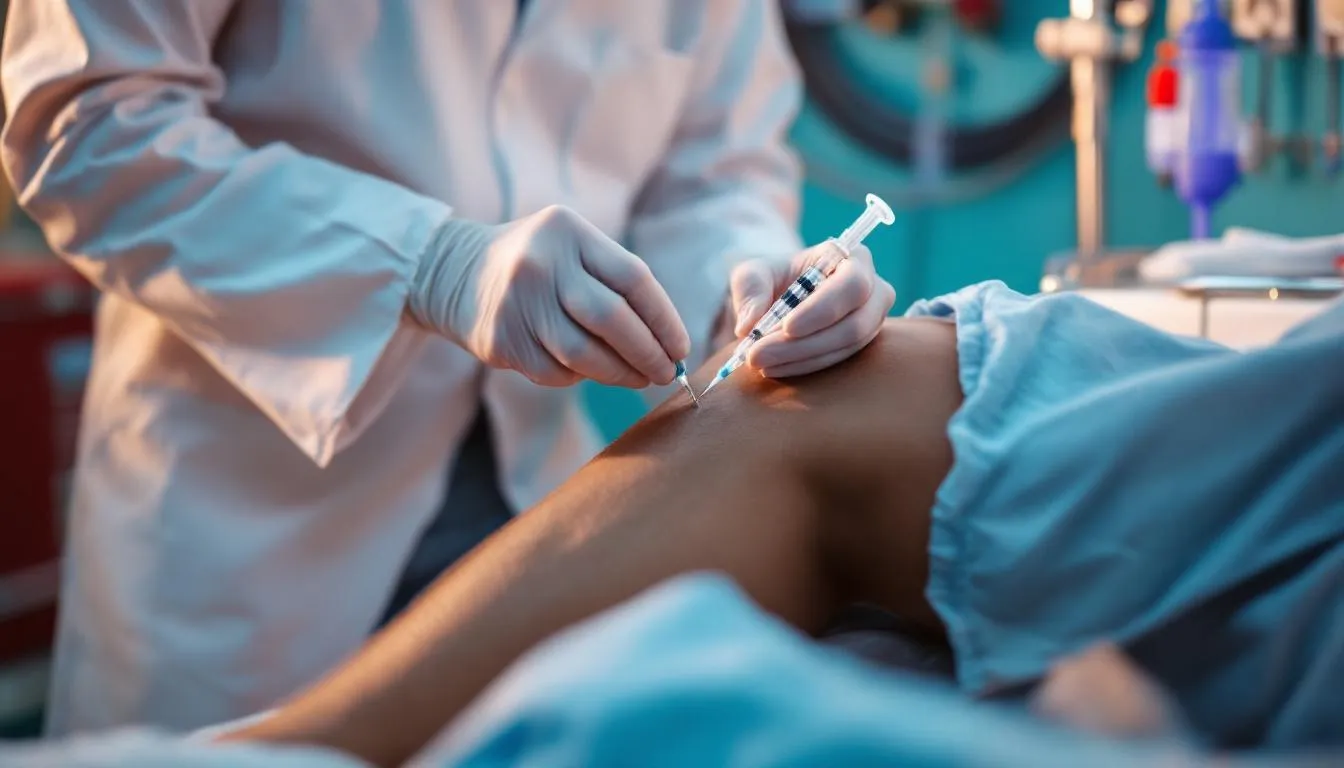
Le PRP représente aujourd'hui le nouveau traitement pour l'arthrose du genou le plus largement utilisé parmi les thérapies biologiques. Le principe repose sur la concentration des facteurs de croissance contenus dans les plaquettes sanguines du patient lui-même. Un prélèvement de sang veineux est effectué, puis centrifugé pour isoler la fraction plaquettaire concentrée, qui est ensuite réinjectée directement dans l'articulation du genou. Ces facteurs de croissance -- TGF-bêta, PDGF, VEGF, IGF-1 -- stimulent la prolifération des chondrocytes, réduisent l'inflammation synoviale et favorisent la synthèse de matrice extracellulaire.
Les données scientifiques accumulées depuis une décennie sont encourageantes. Plusieurs méta-analyses publiées entre 2023 et 2025 confirment que le PRP apporte un bénéfice supérieur à l'acide hyaluronique et aux infiltrations de corticoïdes sur la douleur et la fonction articulaire, avec un effet mesurable pendant 6 à 12 mois après l'injection. Une méta-analyse Cochrane actualisée en 2024 portant sur plus de 3 000 patients a montré une réduction moyenne de 15 points sur l'échelle WOMAC par rapport au placebo. Les résultats sont particulièrement significatifs dans les stades précoces à modérés de la gonarthrose (Kellgren-Lawrence II et III).
Protocole et types de PRP utilisés
Tous les PRP ne se valent pas. Les préparations se distinguent par leur concentration plaquettaire (idéalement 3 à 5 fois la concentration sanguine de base), la présence ou l'absence de leucocytes (PRP leucocytaire vs pauvre en leucocytes), et le mode d'activation. Les études les plus récentes suggèrent que le PRP pauvre en leucocytes (LP-PRP) offre de meilleurs résultats dans l'arthrose du genou, car les leucocytes peuvent libérer des cytokines pro-inflammatoires qui contrecarrent partiellement l'effet thérapeutique. Le protocole standard prévoit généralement une série de 3 injections espacées de 2 à 4 semaines, bien que des protocoles en injection unique avec PRP ultra-concentré soient en cours d'évaluation.
Limites et disponibilité du PRP
Le PRP est disponible en France dans de nombreux centres spécialisés et cabinets de rhumatologie ou de médecine du sport. Il n'est cependant pas remboursé par l'Assurance maladie, ce qui représente un frein pour de nombreux patients. Le coût d'une séance oscille entre 150 et 400 euros selon le centre et le protocole utilisé. Par ailleurs, le PRP ne reconstitue pas le cartilage détruit : il agit principalement comme modulateur biologique de l'environnement articulaire. Dans les formes avancées d'arthrose (Kellgren-Lawrence IV), son efficacité est nettement plus limitée, et les patients relèvent davantage d'une prise en charge chirurgicale par prothèse de genou.
Les cellules souches mésenchymateuses : la promesse de la régénération cartilagineuse
L'injection intra-articulaire de cellules souches mésenchymateuses (CSM) représente l'un des axes de recherche les plus actifs dans le traitement de l'arthrose. Ces cellules, prélevées dans la moelle osseuse (crêtes iliaques), le tissu adipeux (liposuccion) ou le cordon ombilical, possèdent une capacité de différenciation en chondrocytes et exercent un puissant effet paracrine anti-inflammatoire et immunomodulateur. Elles sécrètent des facteurs trophiques qui stimulent les cellules résidentes du cartilage et inhibent les voies de dégradation enzymatique de la matrice.
Plusieurs essais cliniques de phase II et III menés entre 2022 et 2025 ont apporté des résultats prometteurs. L'essai CARTISTEM, utilisant des CSM allogènes dérivées du sang de cordon ombilical, a montré une amélioration significative du score KOOS à 24 mois chez des patients atteints de gonarthrose modérée. L'essai ADIPOA-2, mené en Europe avec des CSM dérivées du tissu adipeux, a démontré une amélioration fonctionnelle durable à 12 mois sans effets indésirables graves. Les analyses IRM de ces essais révèlent, dans une proportion significative de cas, une stabilisation voire une augmentation de l'épaisseur du cartilage articulaire, ce qui constitue un élément inédit dans le traitement de l'arthrose.
Sources de cellules souches et voies d'administration
Le choix de la source de CSM influence significativement les résultats. Les CSM dérivées de la moelle osseuse (BM-MSC) restent la référence historique, mais leur prélèvement est invasif et leur rendement diminue avec l'âge du patient. Les CSM du tissu adipeux (AD-MSC) sont plus faciles à obtenir en grande quantité par liposuccion et conservent un potentiel chondrogène satisfaisant. Les CSM du cordon ombilical ou du placenta, utilisées en allogénie, offrent l'avantage d'une standardisation de la production et d'une activité biologique constante indépendamment de l'âge du receveur. L'injection peut être réalisée en une seule procédure après concentration et expansion en laboratoire, ou combinée à un support biomatériel (scaffold) dans les approches de chirurgie réparatrice.
État réglementaire et accessibilité
En France et en Europe, l'utilisation des CSM dans l'arthrose reste expérimentale et encadrée par les essais cliniques. Aucun produit de thérapie cellulaire n'a encore obtenu d'autorisation de mise sur le marché (AMM) pour cette indication. Au Japon et en Corée du Sud, certains produits à base de CSM (Stemirac, Cartistem) sont commercialisés sous approbation conditionnelle. Les patients français souhaitant bénéficier de ce traitement doivent pour l'instant s'orienter vers les essais cliniques en cours ou vers des centres à l'étranger, avec les précautions que cela impose en termes de suivi médical et de qualité du produit.
Les biothérapies anti-cytokines : cibler les médiateurs de l'inflammation articulaire
L'arthrose n'est plus considérée comme une maladie purement mécanique. La recherche a mis en évidence un processus inflammatoire chronique de bas grade impliquant de nombreuses cytokines et médiateurs pro-inflammatoires. Cette découverte a ouvert la voie aux biothérapies ciblées, déjà utilisées avec succès dans la polyarthrite rhumatoïde, et désormais testées dans la gonarthrose. Deux cibles thérapeutiques ont concentré l'essentiel des efforts : le facteur de croissance nerveuse (NGF) et l'interleukine-1 (IL-1).
Les anticorps anti-NGF : tanézumab et fasinumab
Le NGF est un facteur neurotrophique qui joue un rôle central dans la sensibilisation à la douleur dans l'arthrose. Les anticorps monoclonaux anti-NGF, tels que le tanézumab (Pfizer/Lilly) et le fasinumab (Regeneron/Teva), bloquent l'action du NGF et réduisent de manière spectaculaire la douleur arthrosique. Les essais de phase III ont montré une efficacité analgésique supérieure aux AINS et au placebo, avec une réduction de la douleur de 40 à 60 % chez certains patients souffrant d'arthrose dégénérative sévère.
Cependant, ces molécules ont soulevé des préoccupations de sécurité majeures. Certains patients ont développé une arthropathie destructrice rapide nécessitant une arthroplastie totale du genou, un phénomène attribué à la suppression excessive des signaux douloureux protecteurs de l'articulation. En 2021, la FDA a refusé l'AMM du tanézumab, demandant des données supplémentaires de sécurité. Depuis, de nouvelles études avec des doses réduites et des critères de sélection plus stricts des patients sont en cours. Des résultats intermédiaires publiés en 2024 suggèrent un profil bénéfice-risque amélioré avec l'utilisation de doses faibles chez des patients ne présentant pas de lésions osseuses préexistantes. La décision réglementaire définitive est attendue courant 2026.
L'anti-IL-1 : anakinra et canakinumab
L'interleukine-1 (IL-1) est une cytokine pro-inflammatoire impliquée dans la dégradation du cartilage et l'activation des métalloprotéases matricielles. L'anakinra (Kineret), antagoniste du récepteur de l'IL-1, a été testé en injection intra-articulaire dans la gonarthrose. Les résultats des essais cliniques sont cependant mitigés : si un bénéfice sur la douleur a été observé à court terme (4 à 8 semaines), l'effet ne se maintient pas au-delà de 3 mois dans la plupart des études. Le canakinumab (Ilaris), anticorps monoclonal anti-IL-1 bêta, fait l'objet d'évaluations complémentaires, notamment chez des patients présentant un phénotype inflammatoire marqué (épanchement synovial, CRP élevée). Les chercheurs s'orientent désormais vers des stratégies de ciblage multiple combinant l'inhibition de l'IL-1, du TNF-alpha et de l'IL-6 pour obtenir un effet plus durable sur l'inflammation articulaire.
La thérapie génique : reprogrammer les cellules du genou
La thérapie génique appliquée à l'arthrose du genou vise à modifier génétiquement les cellules de l'articulation pour qu'elles produisent de manière autonome et prolongée des facteurs thérapeutiques. Plutôt que d'injecter régulièrement des médicaments, l'objectif est de transformer les cellules synoviales ou chondrocytaires en véritables usines biologiques capables de sécréter en continu des protéines anti-inflammatoires ou des facteurs de croissance du cartilage.
Le programme le plus avancé est celui de Genascence, avec le produit XT-150, un vecteur viral adéno-associé (AAV) portant le gène de l'IL-10, une cytokine anti-inflammatoire majeure. Après injection intra-articulaire, le vecteur infecte les cellules synoviales qui se mettent à produire de l'IL-10 localement, réduisant l'inflammation sans effet systémique. Les résultats de phase II publiés en 2024 ont montré une réduction significative de la douleur maintenue pendant 12 mois après une injection unique, avec un profil de sécurité acceptable. Un essai de phase III est en cours de recrutement.
Les approches par gène FGF-18 et BMP-7
D'autres approches de thérapie génique ciblent la régénération cartilagineuse en introduisant les gènes codant pour des facteurs de croissance du cartilage. Le FGF-18 (sprifermine) stimule directement la prolifération des chondrocytes et la synthèse de matrice. Le BMP-7 (osteogenic protein-1) favorise la différenciation chondrocytaire et inhibe les effets cataboliques de l'IL-1. Ces approches, encore au stade préclinique ou en phase I, représentent l'horizon thérapeutique le plus ambitieux : la possibilité de restaurer un cartilage fonctionnel par une seule injection. Les défis restent considérables, notamment en matière de contrôle de l'expression génique dans le temps, de ciblage cellulaire précis et de sécurité à long terme.
Les implants de cartilage MACI et la réparation chondrale
La technique MACI (Matrix-induced Autologous Chondrocyte Implantation) représente l'aboutissement de plusieurs décennies de recherche sur la réparation du cartilage articulaire. Elle consiste à prélever un fragment de cartilage sain du genou du patient par arthroscopie, à isoler et multiplier les chondrocytes en laboratoire pendant 4 à 6 semaines, puis à les réimplanter sur une matrice de collagène que le chirurgien fixe sur la zone de lésion cartilagineuse lors d'une seconde intervention. Le produit MACI (Vericel) a obtenu l'approbation de la FDA en 2016 et est utilisé dans plusieurs pays pour le traitement des défauts cartilagineux focaux du genou.
Résultats cliniques et indications
Les données à long terme montrent des résultats encourageants chez des patients bien sélectionnés. Une étude de suivi à 10 ans publiée en 2024 rapporte un taux de satisfaction supérieur à 80 % et une amélioration significative et durable des scores fonctionnels (KOOS, Lysholm). L'IRM de contrôle montre une intégration satisfaisante du néo-cartilage avec un signal proche du cartilage hyalin natif dans la majorité des cas. Toutefois, le MACI est indiqué pour les lésions cartilagineuses focales (défauts délimités de 2 à 10 cm2) et non pour l'arthrose diffuse. Il s'adresse principalement à des patients jeunes ou d'âge moyen présentant un défaut post-traumatique, une ostéochondrite disséquante ou une lésion chondrale focale, dans le but de prévenir l'évolution vers une gonarthrose établie. L'objectif est d'intervenir suffisamment tôt pour arrêter la progression de l'arthrose avant qu'elle ne devienne diffuse.
Les nouvelles générations de scaffolds
La recherche sur les supports matriciels (scaffolds) progresse rapidement. Des biomatériaux de nouvelle génération à base d'hydrogels, de nanofibres de collagène, de soie ou de polymères synthétiques biodégradables sont en cours de développement. Ces scaffolds de troisième génération sont conçus pour mimer la microarchitecture du cartilage natif, avec des gradients de rigidité et de porosité reproduisant la structure en couches du tissu cartilagineux. Certains incorporent des facteurs de croissance à libération contrôlée ou des cellules souches, combinant ainsi réparation structurelle et stimulation biologique. Des essais précliniques chez le gros animal ont démontré la formation d'un tissu cartilagineux de qualité supérieure avec ces nouveaux scaffolds par rapport aux matrices de collagène de première génération.
L'impression 3D de prothèses sur mesure : la chirurgie de précision
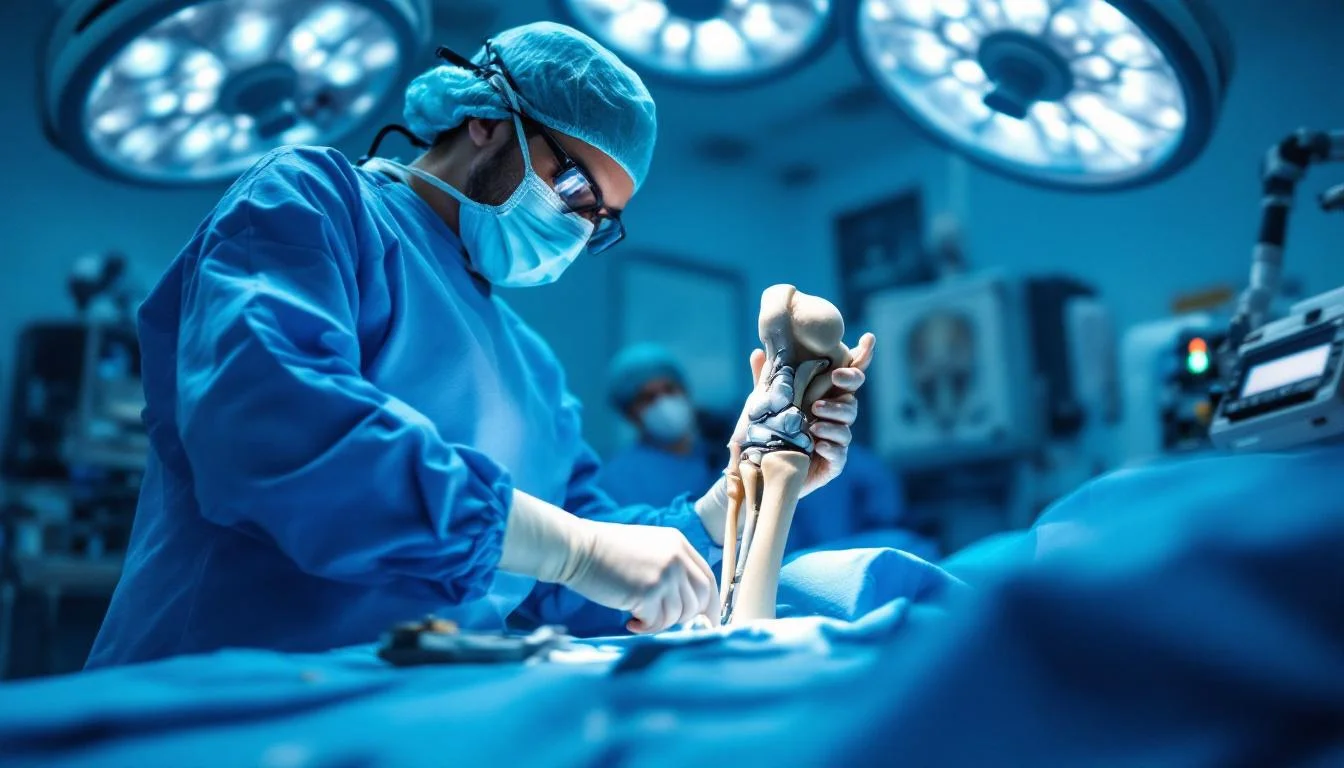
L'impression 3D transforme la chirurgie prothétique du genou. Traditionnellement, les prothèses de genou sont disponibles en un nombre limité de tailles standardisées, ce qui oblige le chirurgien à sélectionner le modèle le plus proche de l'anatomie du patient sans pouvoir garantir une adéquation parfaite. La conséquence est un taux non négligeable de patients insatisfaits après arthroplastie (10 à 20 %), rapportant des douleurs résiduelles, une sensation de genou non naturel ou une instabilité. L'impression 3D permet désormais de concevoir et fabriquer des implants entièrement personnalisés, reproduisant fidèlement l'anatomie articulaire du patient à partir de son imagerie scanner ou IRM.
Processus de fabrication et matériaux
Le processus débute par une imagerie tridimensionnelle haute résolution du genou (scanner ou IRM). Les données sont traitées par un logiciel de planification chirurgicale assistée par intelligence artificielle qui reconstitue un modèle numérique de l'articulation. À partir de ce modèle, un implant unique est conçu pour reproduire les courbures, les reliefs et les dimensions exactes de l'articulation du patient. L'implant est ensuite fabriqué par fusion sélective laser (SLM) ou frittage electron beam (EBM) à partir de poudre de titane, de chrome-cobalt ou de polyéthylène haute densité. Des guides de coupe sur mesure sont également imprimés pour assurer un positionnement optimal de l'implant lors de la chirurgie.
Bénéfices cliniques et perspectives
Les premiers résultats cliniques des prothèses imprimées en 3D sont prometteurs. Les études comparatives montrent une meilleure adéquation implant-os, une cinématique articulaire plus physiologique et une satisfaction patient supérieure par rapport aux prothèses standard. La société Conformis, pionnière dans ce domaine, rapporte un taux de satisfaction à 2 ans de 93 % avec ses prothèses personnalisées iTotal, contre 80 à 85 % pour les prothèses conventionnelles. Plusieurs fabricants majeurs (Stryker, Zimmer Biomet, Smith+Nephew) ont lancé des programmes d'implants personnalisés. Le coût supplémentaire (2 000 à 4 000 euros par rapport à une prothèse standard) reste un frein, mais la tendance à la démocratisation de cette technologie devrait réduire l'écart de prix dans les années à venir. Pour les patients atteints d'arthrose du genou nécessitant une chirurgie prothétique, cette évolution représente un gain qualitatif majeur.
Les exosomes et les hydrogels injectables : les thérapies de demain
Parmi les approches les plus innovantes, les exosomes et les hydrogels injectables se distinguent par leur potentiel à combiner les avantages de la thérapie cellulaire et de la pharmacologie, sans les contraintes de la culture cellulaire ni les risques de la thérapie génique. Ces deux technologies représentent un nouveau traitement pour l'arthrose du genou encore au stade expérimental mais dont les premiers résultats précliniques et cliniques suscitent un intérêt considérable.
Les exosomes : la thérapie cellulaire sans cellules
Les exosomes sont de minuscules vésicules extracellulaires (30 à 150 nanomètres de diamètre) sécrétées par les cellules souches mésenchymateuses. Ils contiennent un cargo biologique riche en microARN, protéines et facteurs de croissance qui reproduisent une grande partie des effets thérapeutiques des cellules souches elles-mêmes. L'intérêt majeur des exosomes réside dans leur absence de cellules vivantes, ce qui élimine les risques de rejet immunitaire, de différenciation incontrôlée et de tumorigenèse. Ils peuvent être produits, standardisés, lyophilisés et stockés, offrant une flexibilité logistique incomparable par rapport aux cellules souches.
Les études précliniques chez le rongeur et le gros animal publiées entre 2023 et 2025 montrent que l'injection intra-articulaire d'exosomes dérivés de CSM réduit significativement les marqueurs d'inflammation synoviale (IL-1, TNF-alpha, MMP-13), stimule la prolifération des chondrocytes et favorise la synthèse de collagène de type II et de protéoglycanes. Plusieurs essais cliniques de phase I/II sont en cours en Chine, au Japon et aux États-Unis. Les premiers résultats chez l'homme, présentés lors du congrès de l'OARSI en 2025, ont confirmé la bonne tolérance du produit et une amélioration clinique à 6 mois chez des patients atteints de gonarthrose modérée.
Les hydrogels injectables : un environnement protecteur pour le cartilage
Les hydrogels injectables représentent une approche distincte mais complémentaire. Il s'agit de biomatériaux polymères (acide hyaluronique modifié, PEG, chitosane, alginate) capables de gélifier in situ après injection dans l'articulation. Ils forment un réseau tridimensionnel hydraté qui remplit les défauts cartilagineux, amortit les contraintes mécaniques et fournit un microenvironnement favorable à la réparation tissulaire. Certains hydrogels de dernière génération sont formulés pour encapsuler des cellules souches, des facteurs de croissance ou des nanoparticules à libération prolongée de médicaments anti-inflammatoires.
L'hydrogel GelrinC (Regentis Biomaterials), composé de PEG et de fibrinogène, est l'un des plus avancés en développement clinique. Injecté sous forme liquide par une simple aiguille, il polymérise in situ sous l'effet de la lumière UV pour former un gel solide qui comble la lésion cartilagineuse. Les résultats de phase II montrent une amélioration clinique significative à 24 mois et une régénération du tissu cartilagineux visible à l'IRM. D'autres hydrogels intégrant des nanoparticules d'anti-inflammatoires (dexaméthasone, triamcinolone) à libération contrôlée sur 3 à 6 mois sont en cours d'évaluation, avec l'objectif de remplacer les infiltrations répétées par une injection unique à effet prolongé.
État des essais cliniques 2024-2025 : ce qui est disponible et ce qui reste expérimental
La multiplication des pistes thérapeutiques dans l'arthrose du genou impose de clarifier ce qui est concrètement accessible aux patients en 2025 et ce qui relève encore de la recherche. Le diagnostic de l'arthrose étant désormais mieux codifié et plus précoce grâce à l'IRM et aux biomarqueurs, la question du timing thérapeutique devient centrale : à quel stade de la maladie quel traitement est-il le plus pertinent ?
Traitements disponibles en pratique clinique
En 2025, les traitements biologiques accessibles en dehors des essais cliniques comprennent les injections de PRP (disponibles largement mais non remboursées), la viscosupplémentation par acide hyaluronique (remboursée sous conditions), et les implants de chondrocytes autologues type MACI (disponibles dans certains centres spécialisés pour les lésions focales). Les traitements conventionnels de l'arthrose du genou -- analgésiques, AINS, kinésithérapie, orthèses, perte de poids -- restent la base de la prise en charge. Les prothèses imprimées en 3D sont disponibles dans un nombre croissant de centres chirurgicaux, notamment dans les CHU et cliniques de référence en chirurgie orthopédique.
Traitements en phase avancée d'essais cliniques (phase II/III)
Plusieurs molécules et produits biologiques sont en phase avancée de développement et pourraient obtenir une autorisation de mise sur le marché dans les 2 à 5 prochaines années. Le tanézumab (anti-NGF) poursuit son évaluation avec un protocole de sécurité renforcé. Le XT-150 (thérapie génique IL-10) est en phase III. Plusieurs produits à base de CSM allogènes (Cartistem, Stemirac) sont en cours d'évaluation en Europe. La sprifermine (FGF-18 recombinant), développée par Merck, a démontré dans l'essai FORWARD de phase II une augmentation significative de l'épaisseur du cartilage à l'IRM, bien que la traduction clinique sur la douleur reste à confirmer en phase III.
Traitements au stade préclinique ou en phase I
Les exosomes dérivés de CSM, les hydrogels injectables chargés en nanoparticules, les approches de thérapie génique ciblant le BMP-7 ou le FGF-18, et les biomatériaux bio-imprimés en 3D mimétiques du cartilage sont au stade préclinique avancé ou en début d'essais chez l'homme. Leur arrivée en pratique clinique est estimée à un horizon de 5 à 10 ans, sous réserve de résultats positifs en matière d'efficacité et de sécurité à long terme. Ces thérapies émergentes modifieront probablement la stratégie globale de prise en charge de l'arthrose, en offrant des alternatives à la prothèse dans des stades où aucune option satisfaisante n'existait jusqu'ici.
Vers une médecine de précision dans la gonarthrose
L'un des enseignements majeurs des essais cliniques récents est que l'arthrose du genou n'est pas une maladie unique mais un ensemble de phénotypes distincts répondant différemment aux traitements. Un patient présentant un phénotype inflammatoire (épanchement, synovite à l'IRM, CRP élevée) ne bénéficiera pas des mêmes thérapies qu'un patient présentant un phénotype mécanique (malalignement, surcharge pondérale) ou un phénotype minimal joint disease. Les biomarqueurs sanguins (CTX-II, COMP, interleukines), l'imagerie avancée (IRM avec cartographie T2, séquences de composition du cartilage) et bientôt l'intelligence artificielle permettront de phénotyper chaque patient et de lui proposer le nouveau traitement pour l'arthrose du genou le plus adapté à son profil. Cette approche de médecine personnalisée représente un changement de paradigme dans la rhumatologie et pourrait considérablement améliorer les taux de réponse thérapeutique, qui restent hétérogènes avec les approches actuelles indifférenciées.